細胞の時間を巻き戻す「CLiP細胞」

今回の治療の鍵は、東京医科大学の落谷 孝広 特任教授らが開発した「誘導性肝前駆細胞=CLiP(Chemically-inducedLiverProgenitors)」だ。これは、成熟した肝細胞に3種類の低分子化合物を加えて培養することで、肝細胞と胆管上皮細胞への二方向分化能を持つ「前駆細胞」へと「若返らせる=時間を巻き戻す(リワインド)」技術である。
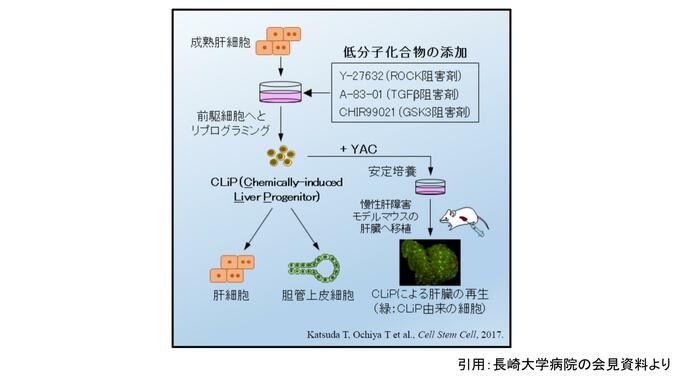
落谷教授は「成熟した肝細胞は通常、体の外では増えませんが、このYACという化合物を用いると、肝細胞がリプログラミング(先祖返り)が起こり、肝前駆細胞(CLiP)になります。CLiPは遺伝子改変をせず、肝臓のアイデンティティを保ったまま一歩手前の状態に戻すことから、iPS細胞等で懸念される腫瘍化(発がん)リスクが極めて低いのが最大の特徴です」と解説した。
また、自身の細胞を用いることから、CLiP細胞を戻した際に拒絶反応が起きにくく、大量に増やせるメリットもあるという。